
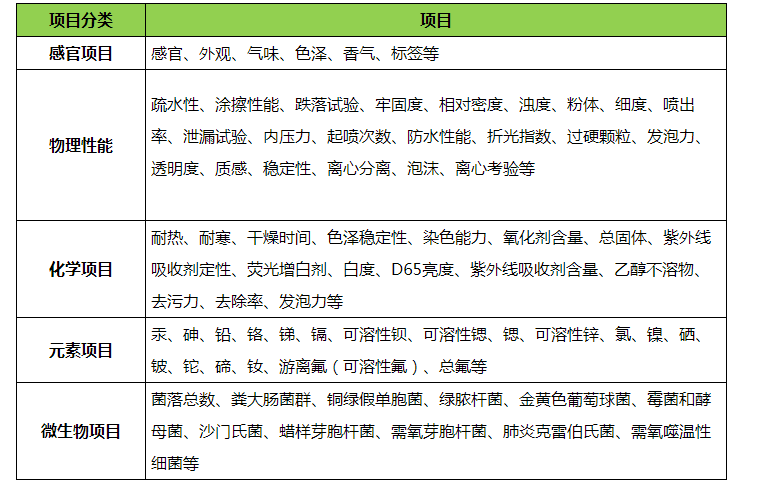
随着人们生活水平的提高,化妆(zhuāng)品逐(zhú)步(bù)进(jìn)入了我们(men)的生活,日常(cháng)生活中我们人人都会(huì)与化妆品接触。由于我们的使用频率较(jiào)高,所以化妆品的质量好(hǎo)坏会影响我们的身体健(jiàn)康,我们需要重视。化妆品检测主要是关注重(chóng)金属、微生物、抗生素、激素、毒理、抗生素(sù)、标准禁止添加项目等。
范围:
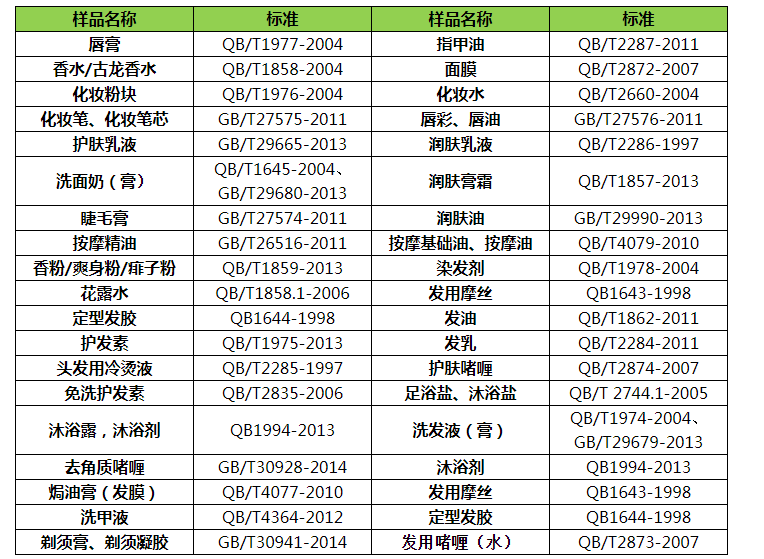
清洁类:牙膏、洗面奶(膏)、洗(xǐ)发(fā)液(膏)、香皂、足
浴盐/沐浴(yù)盐、沐浴剂等
护肤(fū)类:润肤(fū)乳液、润肤膏霜等
滋养类:化妆水、面膜、护发素、发乳、发油等
美容类:化妆粉(fěn)块(kuài)、唇膏、香水/古龙(lóng)水、香粉/爽身粉/痱子粉、定型发胶、发用(yòng)摩丝、染发(fā)剂花露水、指(zhǐ)甲油等

化妆品非特备案
特殊用途(tú)化妆品分别是:育发、染发(fā)、烫发、脱毛、美(měi)乳、健美、除(chú)臭、祛斑(bān)和防(fáng)晒9类化妆品(pǐn),除此之外的化妆品叫做非特殊用(yòng)途化妆品,也就是普通化妆品。
一、凡在中华人民共和国境内生产的非特殊用(yòng)途化(huà)妆品,生产企业应按本规定要求进行产品信息备案。
二、生产企业应当在产品上市销售前,将产品配(pèi)方(不包括含量,限用物质除外)及销售包装(含产品(pǐn)标签、产(chǎn)品说明书)的信息按要求通过统(tǒng)一的网(wǎng)络平台报送至所在(zài)行政区域内的省级食品药(yào)品监管部门。产品安全性评估资料、产品(pǐn)生产工艺简述、产品(pǐn)生产设备清(qīng)单、产品技术要求及(jí)产品检验报告等资料(liào)由生产企业妥善保存备查。
三、委托生产的产品,委(wěi)托双(shuāng)方应(yīng)分(fèn)别向所在(zài)行政区域内的省级食品药品监督管理部门报送(sòng)备案信息。仅供出口的,由实际生产企业向所在行政区域内的省级食品药品监督管理(lǐ)部门报送备案信息(xī)。
四、省级(jí)食(shí)品药品监督管理部(bù)门收到企业的备案(àn)信息后,应当在5个工作日内完(wán)成对备案资(zī)料完整性的核(hé)查(chá)。符合要求的,通过国家食品药品监管总局政务网(wǎng)公布产品备案信息,供公(gōng)众查询。
五、对于不属(shǔ)于(yú)备(bèi)案产品范围的、备案资料不齐(qí)全或备案资料不符合规定形式的,省级食品药品监督管理(lǐ)部门应在5个工(gōng)作日(rì)内告知企业并说明理由。存在明显违法情(qíng)形的,应当责令立即改正,不得上市(shì)销售。
六、省级食品药品监督部门应(yīng)当在备案后三(sān)个月内组织开展对备案产品的实质审查,发现不符合国家相关规定的,应当依法(fǎ)予以查处。
七、已经备案的产品,拟变更原备案事项的,应在变更前将相关变更信息报送备(bèi)案。涉及备案管理部门改变的,应主动申请注销(xiāo)原备案信(xìn)息后,直接申请重新备案。
八、已(yǐ)获备案的产(chǎn)品,自备案之日起每满4年应重新按本规(guī)定要求提交产品(pǐn)备案信息。
九、产品(pǐn)配方信息的报送应符合以下要求:
1.全部原料应详细列明标准(zhǔn)中(zhōng)文名称、原料(liào)序号、限用物(wù)质含(hán)量、使用目的等内容。
2.复配原料应以复配形式填报,应标明(míng)各组分(fèn)的(de)标准中文名称。香(xiāng)精不须列明具体香料(liào)组分的种类和(hé)含量。
3.原料(含复配原料中的各组分)应按《国(guó)际化妆品原料标准中文名(míng)称目(mù)录(lù)》使用标准中文名称,无国际化妆品原料名称(INCI)或未列入《国际化(huà)妆品原料标准中文名称目录》的,应(yīng)使用《中国药典》中的名(míng)称或化学名(míng)称或植物拉丁(dīng)学名,不得使用商品名或俗名,但复配原料除外。
4.着色剂应提供《化妆品(pǐn)卫生规范》中载明的着色剂索引号(简称CI号),无CI号的除外。
5.凡在产品配方中使用(yòng)来(lái)源于石油、煤焦油的碳(tàn)氢化合物(wù)的(单一组分(fèn)的除外),应标明相关原料的化学文摘索引号(简(jiǎn)称CAS号)。
6.使(shǐ)用动物脏器组织及血液制品提取物的原料,应当收集该(gāi)原料(liào)的来源、质量规格和原料生(shēng)产国允许使用的证明等资料存档备查。
7.使(shǐ)用《化妆品卫(wèi)生规范》对(duì)限用物质有规格要求的(de)原料,应当收集该(gāi)原料生产(chǎn)商出具的原料质量规格证明存档备查。
8.宣称为儿童或(huò)婴儿使用(yòng)的产品,配(pèi)方设计原则(含(hán)配方整体分析报告)、原料的选择原则和要求、生产工艺、质量控制等内容应当按照《儿童化妆品(pǐn)申(shēn)报与审评指南》(国食(shí)药监保(bǎo)化[2012]291号)的要求编制(zhì),相关资料应当存档备查。
9、产品技术要(yào)求的编制参(cān)照(zhào)《关于印发化妆品产品技术要求规范(fàn)的通知》(国食药监许[2010]454号)要求执行;检验要求参照《关于印发化妆品行政许可检验管理办法的(de)通知》(国食药监许[2010]82号)执行,其中企业参照《关于(yú)印发化妆品中可能存在(zài)的安全性风险物质风险评估指南的通(tōng)知》(国食(shí)药监(jiān)许[2010]339号)要求进(jìn)行风险评估并(bìng)确认产品(pǐn)安全性的(de),可免做毒理相关(guān)检测。
浙江和诺检测(cè)技(jì)术有限公司可以(yǐ)提供(gòng)样品送检服(fú)务,进行非特备案的咨询和指导。
欧盟CPSR(化妆品安全报告)
CPSR(化妆品安全报(bào)告)是产品进入欧盟市场的通行证(zhèng),欧(ōu)盟化妆品新法规Regulation(EC)1223/2009已于2013年7月11日正式实施(shī),相比于之前的化妆品指令Directive 76/768 EEC,对化妆品的(de)安全(quán)性提出了更加严格的要求(qiú),其中明确规定了产品必须(xū)完成化妆品安全报告(Cosmetic Product Safety Report,CPSR)后方能够在欧盟经济区上市销售。
根据新法规,欧洲化妆品协会(原Colipa)和欧盟委(wěi)员会共同制定了化妆品安全(quán)报告指(zhǐ)南,详(xiáng)细解读和列出了法规中关于CPSR的要求。该指南文(wén)件于2013年11月 25日由欧盟委员会作为委员会决议(Commission Decision)发布,欧盟委员会决议(yì)具有法律效率,因此企(qǐ)业必须遵从该决议。目(mù)前(qián)进(jìn)行的毒理学(xué)风险评估(Toxicological Risk Assessment,TRA)以(yǐ)及类似的简(jiǎn)单升级版本已经不能够满(mǎn)足CPSR以及该指南的要求。指南更加细化了新法规关于CPSR的要求。增加的重要细则如(rú)下:
1. 产品配方中的各(gè)组分需提供准确的含量,若无法提供定量信(xìn)息则按照高剂量计算。复杂(zá)成分如(rú)提取物或生物制品等需提供纯度标准及测试方法。
2. 产品中使用的原材料供应商(shāng)须在报告中指(zhǐ)出(chū),香料和香精必须提(tí)供生(shēng)产商和产品代码信息。
3. 化妆品包装材料需要(yào)满足食品接触材料(Food Contact Material)的标准并保证其稳定(dìng)性。特别对(duì)于一些对光和空气敏感的(de)产品,其正确的贮存方法需要在标签上得以体现。
4. 产品需要提供稳定性(Stability)报(bào)告,其中(zhōng)包括稳定性测定方法,防腐剂挑战试(shì)验报告,产品有效期(qī)以及开盖使用日期(Period-after-opening)。
5. 化妆品微生物方面的要求进一步细化,高风(fēng)险的原料(liào)需要(yào)注意微生物危害。
6. 化妆(zhuāng)品原料以及其包材中可能含有(yǒu)的杂质需要(yào)进行风(fēng)险(xiǎn)评估并证明其技(jì)术上是(shì)不可避免的(如GMP条件下也无法避免)。
7. 化妆品所使用的原料需要提供详细的毒理档案(Toxicological Profile of Substance,TPS),每一个原料需要提供(gòng)其毒理学信息(xī),包(bāo)括急性毒性(xìng)、刺(cì)激性、过敏性等(děng)共12项毒理学端点。
8. 化妆品原材料(liào)和(hé)成品的生产商都需要达到GMP(ISO 22716)标准。 由于原料中的杂质(zhì)具有潜在的可以影响物质毒性的风险因素,因此(cǐ)在评估杂质的安全性时可以引入毒理学关注阈值(TTC)作为(wéi)有(yǒu)效的评估(gū)手段。
9. 若出(chū)现不良反应,则(zé)需在报告中评估其发生的(de)可能性和因果关系,出现严重的不良反应需上报(bào)欧盟(méng)成员国有关主管部门,并在CPSR报告中(zhōng)以附件(jiàn)形式(shì)存在并描述处理和解决方法。
10. 在评估(gū)报告结论中必须提到新(xīn)的化妆品法规Regulation(EC)1223/2009,并且明确(què)指出产品是否符(fú)合新的(de)化妆品法规(guī)。
11. 关(guān)于产品标签,警告用(yòng)语和使(shǐ)用说明在满足新法规外还须参(cān)考相关文件,如 Commission Recommendation 2006/647/EC 及其它与标签相(xiàng)关的指导文件。为了直观地表达该内容,可以在CPSR中附上产品的图片(piàn)。
12. 毒理风险评估由定性评估变为定量评估。包括产(chǎn)品系(xì)统性的风险评(píng)估,配方组合后的兼容性,稳定性,微生物,包(bāo)装,标签以及使用等各个方面。产品所有的测试报告、技术文档和其它相(xiàng)关信息须经过毒理风险评估师(shī)评估,并特别注意三岁以(yǐ)下儿童使用的产品,除了满足新法规(guī)要求还需遵循欧盟消费者安全科学委员会(SCCS)指南。
13. 当法律要求出现变化(huà)或更改时,产品的原材料发生改变(如更换供应商),使用条件发生(shēng)改变,以(yǐ)及(jí)监测到在正常使用条件下不良反(fǎn)应(yīng)发生率增(zēng)加时,毒理风(fēng)险评估师须对产品进行重新评估,确保化(huà)妆品安全报告(CPSR)保持同步更新并满足新法规要求。
14. 指南对于可以出具化妆(zhuāng)品安全报(bào)告(CPSR)的安全评估师资质做了详细的定义,非欧盟成员国承认(rèn)的药学,毒理(lǐ)学等相关专业人员不得从事化妆品安(ān)全报告评(píng)估工作。并且评估(gū)师的资质及相关学历证明需要附在评估报告后。
相关信(xìn)息/ RELATED INFO
MORE
服(fú)务(wù)热(rè)线
微信扫一扫


返回顶部